Mes premières observations — de lames préparées par mes soins — sont loin d’être aussi intéressantes que je l’espérais, et c’est normal ! Je n’ai que de vagues connaissances théoriques et virtuellement aucune pratique. Les premières préparations ne seront peut-être jamais parfaites, elles présentent néanmoins l’intérêt d’être les premières, et en soi, c’est un accomplissement personnel. En outre, j’ai pu voir quelques points à faire ou ne pas faire, et identifier ses erreurs fait partie du parcours initiatique.
Des conditions suboptimales
Je voulais me faciliter la vie en utilisant un échantillon liquide (pour ne pas commencer à sculpter la moelle de sureau et utiliser le microtome sans m’y familiariser un peu) : j’ai deux bacs dans le jardin remplis d’eau de pluie et à ciel ouvert. En octobre, j’en avais déjà rapporté un prélèvement et observé une vie fourmillante, mais je n’ai pas enregistré ces observations. Je m’attendais donc à un résultat similaire aujourd’hui.
On sort tout juste de plusieurs jours de gel avec des températures inférieures à -4℃. Les bacs étaient couverts d’une couche de glace, mais pas complètement gelés.
La température extérieure actuelle est de 14℃. J’espérais que deux jours à cette température auraient suffi à ce que la vie reprenne de façon spectaculaire dans ces bacs. Malheureusement, mon échantillon s’avéra relativement désert. J’imagine que j’aurai dû attendre de nouvelles pluies avant de faire mon prélèvement.
Je note également que, si je continue à utiliser l’iPhone, je vais devoir faire quelques paramétrages pour obtenir des prises de vue de meilleure qualité.
De l’importance du matériel
Si je me suis bien équipé de gants et d’une blouse, il me manque encore un peu de matériel pour utiliser tout cela avec plus de confiance.
- Des micro-pipettes (éventuellement jetables) : je manque d’habileté avec mes grosses pipettes actuelles, idéales pour prélever l’échantillon depuis un récipient un peu profond (tel que mes bacs d’eau de pluie) mais effectivement inadaptées pour déposer une goutte correctement centrée sur la lame.
- Des buvards : les colorants de laboratoire sont très puissants. Les buvards sont indispensables pour éliminer l’excédent de colorant ou de l’échantillon liquide qui va immanquablement s’écouler aux bords de la lamelle.
Je me suis aussi procuré de petits plateaux dont je me sers pour préparer le matériel avant usage, et pour protéger mon plan de travail. Ils se sont avérés très pratiques à l’usage, permettant de garder tout ce dont j’ai besoin sous la main tout en évitant que les colorants se répandent en cas de pépin.
Syndrome de l’imposteur
En me relisant, un sentiment assez perturbant commence à naître en moi : la peur d’être jugé. Je n’y connais rien, je n’ai pas de formation. Quand on voit certains faire des vidéos de microbiologie sur Internet, on voit clairement qu’ils ont accès à un vrai laboratoire, avec des équipements adaptés. Moi, je fais ça sur un coin de lavabo, trop bas et trop étroit pour être confortable. Comment ne pas me dire que je suis ridicule ?
Cependant :
- qui va me faire une réflexion, sinon les haters ? (encore faudrait-il qu’ils tombent sur mon site et sur un formulaire de contact que je n’ai toujours pas créé 😈)
- démarrer une nouvelle activité va toujours de pair avec l’incertitude : ce n’est pas ça qui va m’arrêter
- j’apprends, que ce soit grâce aux ratés comme aujourd’hui ou grâce aux réussites ultérieures ; c’est apprendre qui est le plus important pour moi
Il faut aussi garder en tête un point très particulier : je ne contribue pas à sauver des vies. Si je mets trop de colorant, on ne va pas rater une infection bactérienne potentiellement létale.
Donc, oui, je suis un amateur. Oui, je suis mal équipé et mal meublé. Oui, je vais faire des erreurs et affronter les déceptions.
Rien que je n’ai déjà connu par le passé dans ma carrière de développeur.
J’ai envie de dire : c’est OK d’avoir le syndrome de l’imposteur, de ne pas se sentir légitime. Au pire, cela prouve que je ne suis pas arrogant, et au mieux, cela m’incite à continuer pour m’améliorer, et améliorer mes observations.
Protocole
Afin d’éviter un défaut présent sur la caméra fournie avec mon microscope, j’ai acquis un support premier prix pour mon iPhone. Il devait me permettre de tester cette association. Malheureusement, il réduit significativement le champ de vision, en plus de provoquer des aberrations chromatiques.
Comme j’utilise l’iPhone, je ne peux pas utiliser le logiciel proposé par Swift. En l’absence d’une solution satisfaisante, je me suis contenté de QuickTime complété par iMovie. Je suis donc toujours à la recherche d’une stack logicielle convaincante, à la hauteur de Swift Imaging.
J’utilise mes lames concaves afin de préserver les mouvements naturels des créatures qui pourraient se trouver dans l’échantillon. Une conséquence un peu embêtante des lames concaves est la difficulté de mise au point : les organismes motiles (capables de mouvement) bougent aussi sur le plan vertical et donc la mise au point doit se faire en temps réel. C’est un exercice en soi qui explique donc au moins en partie pourquoi mes premières prises de vue sont occasionnellement nettes… Ça, et le fait que je suis plus habitué aux déplacements au clavier et au TrackPad qu’avec une paire de molettes.
J’ai donc préparé quatre lames :
- une sans aucun colorant
- une avec du bleu de méthylène
- une avec de l’éosine
- une avec de la fuchsine
Après avoir déposé, tant bien que mal, une goutte de l’échantillon dans la cavité de la lame, j’y ai ajouté une goutte de colorant, puis j’ai déposé une lamelle couvre-objet par-dessus, en m’efforçant de limiter les bulles d’air : c’est plus difficile à faire que sur une lame plate, et quelques bulles seront visibles.
Lame brute
La lame brute est préparée sans colorant. Les couleurs des organismes sont vraies, et il est fascinant d’en voir d’aussi vives sous le microscope, sans technique spécifique.
Je suis tombé assez rapidement sur un cluster inédit de quatre individus de l’espèce que j’avais principalement découverte dans mon échantillon datant d’octobre.
Du moins, je pense que ce sont quatre individus, même s’ils semblent partager une membrane commune.
Un cluster de quatre organismes. Couleurs naturelles.
Un peu plus loin, j’ai pu observer un individu isolé et immobile. Ses couleurs naturelles me laissent penser qu’il est dormant ou mort tardivement pendant la préparation.
Organisme non identifié présent dans mon échantillon d’eau stagnante. On peut apercevoir la membrane tout autour. Couleurs naturelles.
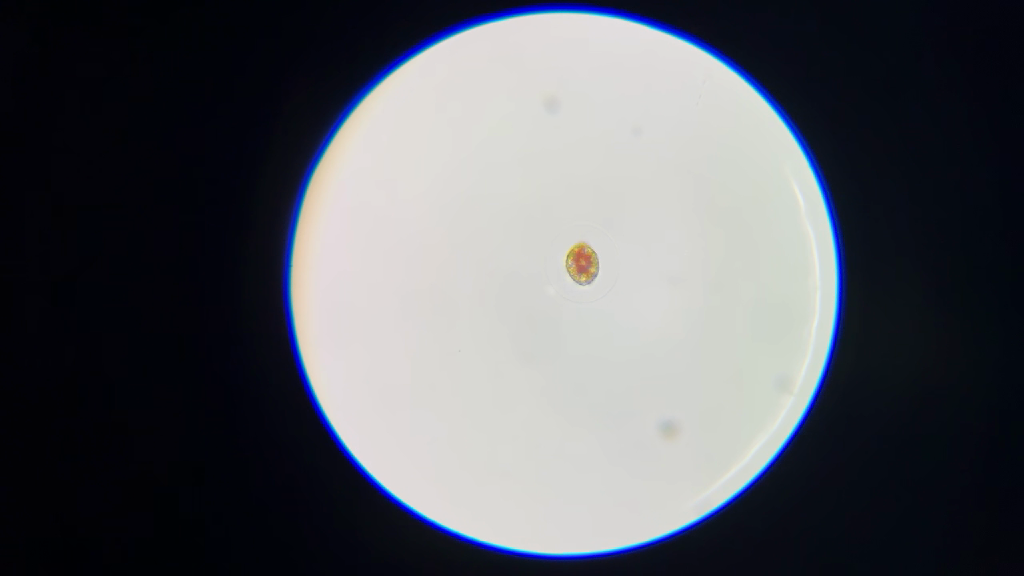
Bleu de méthylène
Ces organismes colorés au bleu de méthylène prennent des couleurs étonnantes : du bleu, évidemment, mais aussi un bel orange qui est en réalité la pigmentation naturelle de l’organisme, comme on l’a vu sur la lame brute. On en déduit que les éléments colorés en bleu contiennent des substances acides (sans doute de l’ADN ou de l’ARN), et que les éléments non colorés pourraient être des vacuoles.
L’un des organismes coloré au bleu de méthylène.
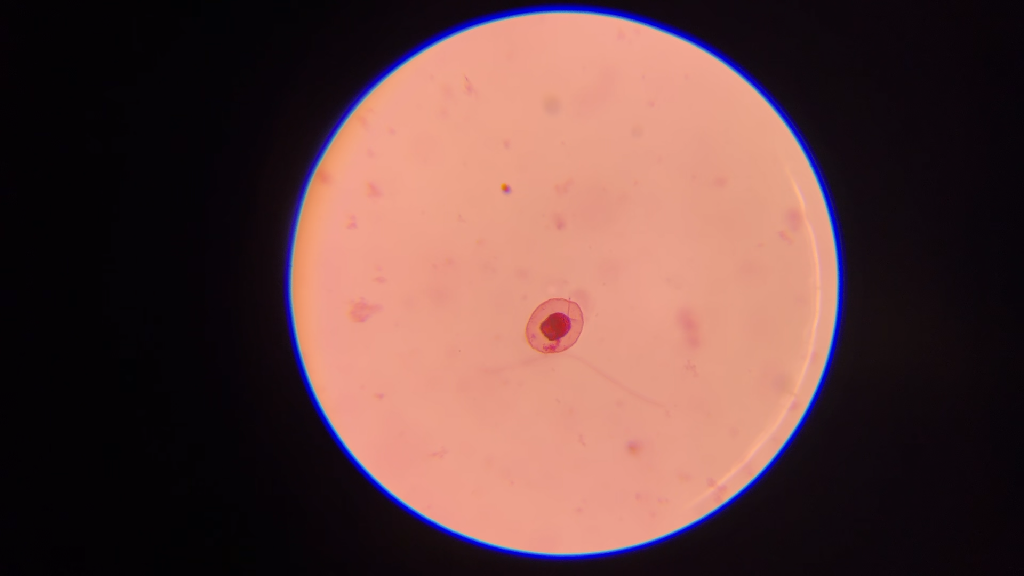
Fuchsine
Il est clair que j’ai raté la coloration à la fuchsine en omettant de la re-doser avant application, ou tout simplement parce qu’elle n’est pas adaptée à cet échantillon.
Néanmoins, elle met en évidence la membrane externe de l’organisme, ainsi que ses deux “antennes” intérieures. Le reste est malheureusement trop saturé de colorant pour y déceler quoique ce soit d’intéressant à mes yeux d’observateur candide.
La fuchsine, bien que saturée, met bien en évidence ici la membrane de l’organisme, ainsi que ses “antennes”.
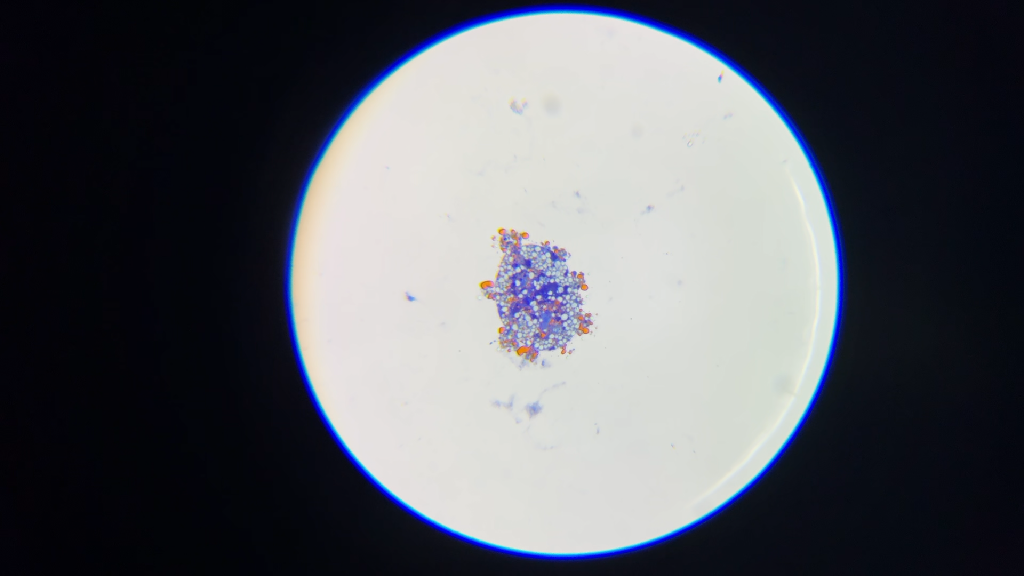
Éosine
J’ignore si c’est spécifiquement l’éosine qui a fait apparaitre ces structures, mais j’ai pu découvrir des éléments qui ressemblent vaguement à du corail.
Ces structures se retrouvent un peu partout sur la lame et ne semblent révélée que par l’éosine. La lame à l’éosine est la dernière que j’ai observé. J’ai nettoyé trop hâtivement les autres lames, ne me laissant pas le loisir de vérifier si ces structures y étaient présentes et visibles.
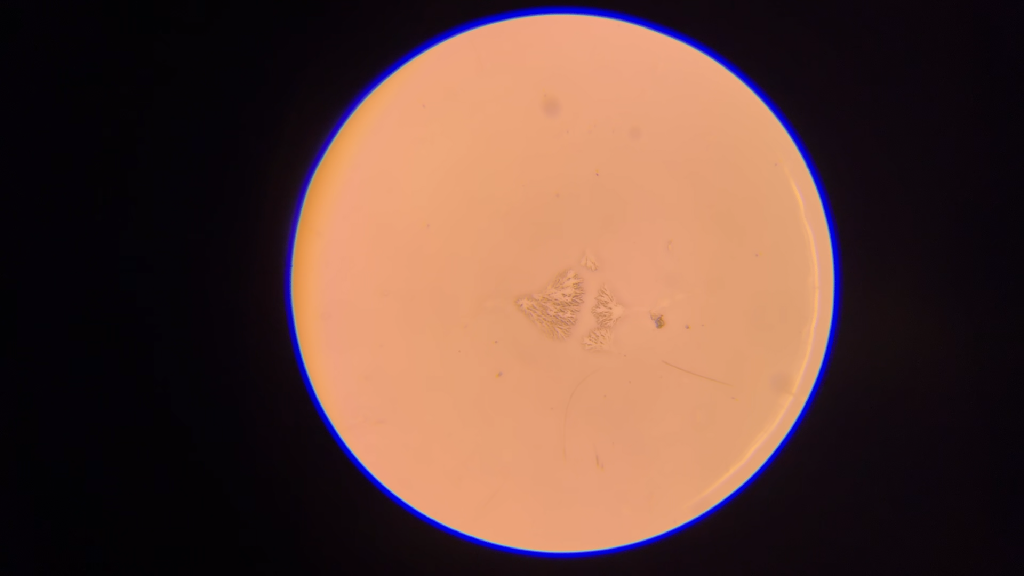
Je constate d’ailleurs que l’éosine a été moins fatale aux organismes que ne l’ont été le bleu de méthylène et la fuchsine. J’ai pu observer un individu isolé, mais vigoureux, et une autre grappe de quatre individus, eux aussi plutôt vigoureux puisqu’ils ont passé leur temps à nager dans leur membrane commune.
Dur de suivre ce petit organisme ! La coloration à l’éosine ne semble pas l’avoir affecté. Notez que, outre ma difficulté à le garder dans le cadre, il faut garder à l’esprit que dans une lame concave, il peut aussi se balader sur le plan vertical : ça fait trois molettes avec lesquelles jouer. Vivement que je puisse m’équiper d’une platine motorisée !
Un cluster de quatre organismes colorés à l’éosine. La membrane partagée est mieux visible. On peut également distinguer les “antennes”.
Interprétation des observations
Comme j’avais déjà observé cette eau il y a quelques mois, je savais plus ou moins ce que j’allais y trouver. Il y a donc au moins un organisme que j’ai pu revoir (sans être encore capable de l’identifier), et que je cherchais activement sur mes lames.
D’abord surpris par le vide de mes échantillons, j’ai finalement pu voir avec satisfaction que cet organisme était présent sur les quatre lames. Et, contre toute attente, j’ai observé quelque chose de nouveau : des agrégats de quatre de ces organismes sur différentes lames. Je n’ai observé aucun agrégat de plus ou de moins de quatre individus.
Pouvoir interpréter ses observations est important, et force est de constater que j’en suis encore incapable. Effectivement crucial dans le cadre de la médecine, c’est beaucoup moins central dans le contexte du hobby. Néanmoins, pour ma culture personnelle, j’aimerais réussir à déterminer ce que j’ai vu.
Notamment :
- quelle est donc cette créature, avec ses deux “antennes” situées à l’intérieur de sa membrane ?
- pourquoi ai-je observé des agrégats de quatre individus qui semblaient se trouver dans la même membrane ? aurais-je donc assisté à une séance de cannibalisme ou de reproduction ? ou bien était-ce un comportement grégaire dû à la perturbation de leur environnement ?
Et, moins directement : est-ce que le vide relatif de mes lames est effectivement dû aux conditions particulières que j’ai décrites plus tôt ?
Certaines de ces réponses pourraient m’être données rapidement par n’importe quel biologiste, mais j’aime l’idée que je puisse y répondre par moi-même : il me suffit de prélever un nouvel échantillon à une période de l’année plus propice (dans un ou deux mois). Je saurai alors si la fluctuation du nombre d’organismes présents dans mes bacs est fonction de l’environnement.
L’identification de la bestiole posera sans doute plus de problèmes, ce qui est une bonne chose : il se trouve que j’ai aussi envie d’apprendre la description scientifique. Si je deviens capable de la décrire correctement (avec le vocabulaire adéquat), il devrait m’être d’autant plus facile de l’identifier.
Conclusion
- Dire que j’ai raté une préparation, mais que cela contribue à mon apprentissage, n’est pas un truc de looser : j’ai effectivement acquis mes premières notions de préparation de lames, notamment en mettant trop de colorant et en me précipitant un peu.
- Il faut être patient et méticuleux. Je le suis à l’extrême dans les domaines que je maîtrise, mais l’enthousiasme me fait faire des erreurs dans les domaines que je découvre.
Une chose est certaine, c’est que j’aime beaucoup utiliser les colorants. Dans mon précédent article, je précisais que leur usage ne devait pas être systématique et je n’ai pas changé d’avis sur la question. Néanmoins, je pense qu’il y a des choses à faire avec, dans un cadre plus artistique que scientifique.
Attention à un point que je découvre : les colorants et réactifs (et/ou leur conditionnement) dégagent de fortes odeurs. En l’occurrence, mes produits chimiques m’ont été expédiés dans un sachet plastique scellé. Ce n’est qu’au déballage que j’ai pu me rendre compte d’une puissante odeur émanant probablement du flacon d’eau iodée. Le problème se résout facilement en nettoyant l’extérieur du flacon, et en aérant la pièce dans laquelle il se trouve. Aucune fuite n’est à déplorer : j’en déduis que c’est au remplissage du flacon qu’un peu de solution a peut-être coulé à côté.
Pas de quoi s’inquiéter, cela fait partie des réflexes à avoir pour bien manipuler ses produits. J’aurais dû les déballer plus vite et les stocker dans un contenant approprié (une boite en verre par exemple).
Je pense que je vais prendre l’habitude de colorer tous mes prélèvements, tout en variant les colorations. Ici, j’ai voulu tester “vite fait” chaque colorant indépendant les uns des autres, mais la prochaine fois, je préparerai une lame mêlant bleu de méthylène et éosine.
Je pense aussi que je vais limiter l’usage des lames concaves (qui sont de toute façon très chères). Cela devrait me simplifier certaines prises de vue si je n’ai pas besoin d’ajuster l’axe vertical en permanence, et me permettre de passer à un grossissement plus élevé.

